Nat Commun:突破哺乳动物细胞定向进化瓶颈!PROTEUS平台开启蛋白工程研究新纪元
来源:生物谷原创 2025-07-10 14:00
PROTEUS平台的问世为哺乳动物细胞内的蛋白质定向进化提供了全新的解决方案。相较于传统系统而言,该平台在稳定性、突变率、筛选效率和功能多样性方面均表现出显著优势。
在合成生物学和基因工程快速发展的今天,定向进化(DE,Directed Evolution)已成为改造蛋白质功能的核心技术之一。通过模拟自然选择的过程,研究人员就能在实验室中“演化”出具有特定功能的蛋白质,其广泛应用于药物开发、基因治疗、生物传感器等领域。然而,现有的定向进化平台大多依赖于原核生物或酵母系统,这些系统虽然操作简便,但缺乏哺乳动物细胞中复杂的翻译后修饰、蛋白互作网络和信号调控机制,限制了其在人类疾病研究和治疗中的应用。
近年来,随着CRISPR、RNA干扰、病毒载体等技术的成熟,科学家开始尝试在哺乳动物细胞中建立定向进化系统从而获得更贴近人类生理环境的蛋白质变体;然而,哺乳动物系统的稳定性差、突变率低、筛选效率低等问题始终制约着这一领域的发展。因此,开发一种高效、稳定、适用于哺乳动物细胞的定向进化平台,成为当前生命科学研究的重要前沿课题。
近日,一篇发表在国际杂志Nature Communications上题为“A chimeric viral platform for directed evolution in mammalian cells”的研究报告中,来自悉尼大学等机构的科学家们通过研究开发出了一种名为PROTEUS(PROTein Evolution Using Selection)的新型定向进化平台,这一平台基于一种嵌合病毒样囊泡(Virus-Like Vesicles, VLVs)系统,其能在哺乳动物细胞中实现多轮、稳定的蛋白质定向进化,从而就能突破传统系统的技术瓶颈。
文章中,研究人员以塞姆利基森林病毒(SFV,Semliki Forest Virus)为基础构建了一种不含衣壳蛋白的病毒复制子系统,该系统能通过宿主细胞表达水泡性口炎病毒G蛋白(VSVG)来实现病毒的包装与传播从而避免了传统病毒系统中衣壳蛋白与病毒RNA之间的相互作用所带来的“作弊粒子”问题。这种设计不仅能提高系统的稳定性,也使得每一轮进化都可以在“新鲜”的宿主细胞中进行,并能避免宿主基因组突变对实验结果的干扰。
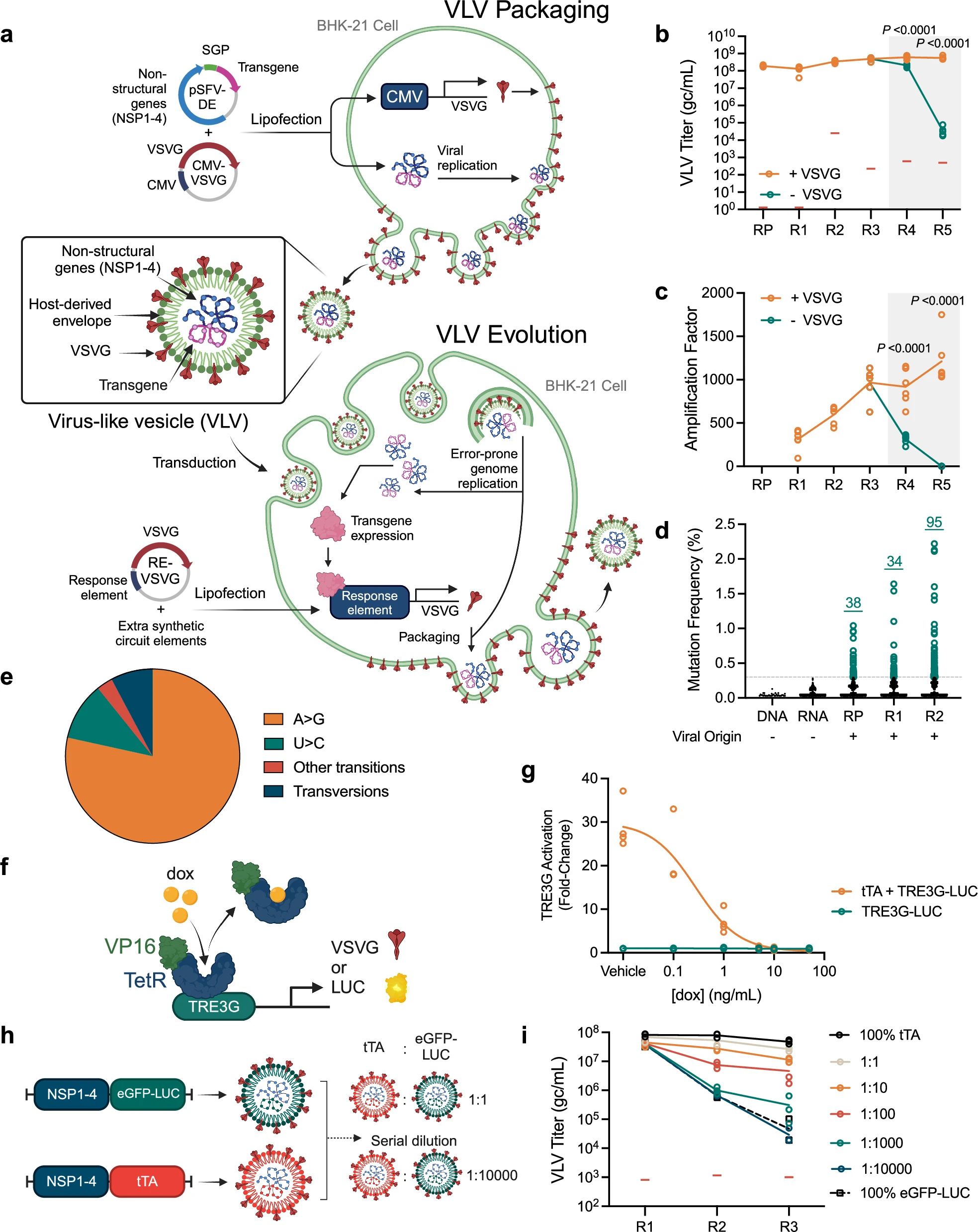
嵌合病毒样囊泡的宿主依赖性传播
在实验流程上,研究人员首先将目标蛋白基因插入SFV复制子中,并与VSVG表达载体共转染至BHK-21细胞中从而生成VLVs;随后这些VLVs被用于感染表达特定筛选回路的新宿主细胞。只有当目标蛋白具备所需功能时才能激活VSVG的表达从而支持VLV的复制与传播,通过多轮感染与筛选,该系统就能富集出功能更优的蛋白变体。
研究人员在多个实验中验证了PROTEUS平台的实用性与高效性,首先他们对四环素调控转录激活因子(tTA)进行进化成功获得了对多西环素(doxycycline)更具耐受性的变体;其次对第三代反式激活因子rtTA-3G进行优化得到了灵敏度更高、泄漏表达更低的TetON-4G系统,其适用于人类诱导多能干细胞衍生的类器官模型。此外,研究人员还利用该平台对一种抗p53纳米抗体进行进化,从而就能显著提升其在DNA损伤响应中的核定位能力,同时还成功构建出一种可用于活细胞成像的p53生物传感器。
研究者指出,PROTEUS平台还展现出良好的突变多样性和可控性,该系统能利用SFV本身高错误率的RNA复制机制并结合宿主细胞中的ADAR酶编辑活性,从而就能实现每轮约2.6×10⁻⁵的突变频率。此外,研究人员还通过引入RNA核苷类似物molnupiravir,将突变率提高了8倍并改变了突变谱系,这就为未来的进化策略提供了更多可能。
PROTEUS平台的问世为哺乳动物细胞内的蛋白质定向进化提供了全新的解决方案。相较于传统系统而言,该平台在稳定性、突变率、筛选效率和功能多样性方面均表现出显著优势;其嵌合病毒设计不仅解决了系统污染和“作弊粒子”问题,也使得多轮进化成为可能,从而极大地拓展了可进化的蛋白种类和功能空间。未来,随着对哺乳动物细胞系统理解的深入,PROTEUS有望在基因治疗、抗体工程、合成生物学等领域发挥更大作用。(生物谷Bioon.com)
参考文献:
Cole, A.J., Denes, C.E., Moreno, C.L. et al. A chimeric viral platform for directed evolution in mammalian cells. Nat Commun 16, 4250 (2025). doi:10.1038/s41467-025-59438-2
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


